Физико-химические свойства вещества
Окись углерода представляет собой бесцветный лишенный запаха газ, который имеет низкую плотность по воздуху (0.97), замерзает при температуре -204° В воде и в плазме крови растворяется очень мало - около 2% ( по объему), но в спирте в 10 раз больше. Особенностью окиси углерода является тот факт, что окись углерода не адсорбируется пористыми материалами. Является восстановителем, вступает в реакции окисления. Горит синим пламенем с образованием двуокиси углерода – СО2. Такая реакция может идти без нагревания в присутствии катализатора, например гопкалита.
Получают двумя способами:
1. В промышленности при взаимодействии раскалённого угля с углекислым газом: С + CO2 = 2CO или водяным паром: С + H2O = CO + H2. Таким образом, производят генераторный и водяной газы, использующиеся как газообразное горючее.
2. В лаборатории CO получают нагреванием при 100°С муравьиной кислоты с серной кислотой; при этом происходит реакция: HCOOH = H2O + CO.
Промышленный способ
1. Образуется при горении углерода или соединений на его основе (например, бензина) в условиях недостатка кислорода:
2C + O2 → 2CO↑ (тепловой эффект этой реакции 220 кДж),
2. или при восстановлении диоксида углерода раскалённым углём:
CO2 + C ↔ 2CO↑ (ΔH=172 кДж, ΔS=176 Дж/К).
Эта реакция часто происходит при печной топке, когда слишком рано закрывают печную заслонку (пока окончательно не прогорели угли). Образующийся при этом монооксид углерода, вследствие своей ядовитости, вызывает физиологические расстройства («угар») и даже смерть (см. ниже), отсюда и одно из тривиальных названий — «угарный газ». Картина протекающих в печи реакций приведена на схеме.
горение пожароопасный тушение
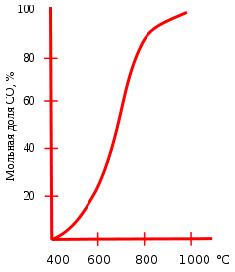
Реакция восстановления диоксида углерода обратимая, влияние температуры на состояние равновесия этой реакции приведено на графике. Протекание реакции вправо обеспечивает энтропийный фактор, а влево — энтальпийный. При температуре ниже 400 °C равновесие практически полностью сдвинуто влево, а при температуре выше 1000 °C вправо (в сторону образования CO). При низких температурах скорость этой реакции очень мала, поэтому монооксид углерода при нормальных условиях вполне устойчив. Это равновесие носит специальное название равновесие Будуара.
3. Смеси монооксида углерода с другими веществами получают при пропускании воздуха, водяного пара и т. п. сквозь слой раскалённого кокса, каменного или бурого угля и т. п.
Лабораторный способ
1. Разложение жидкой муравьиной кислоты под действием горячей концентрированной серной кислоты, либо пропуская муравьиную кислоту над оксидом фосфора P2O5. Схема реакции:
HCOOH →(t, H2SO4) H2O + CO↑
Можно также обработать муравьиную кислоту хлорсульфоновой. Эта реакция идёт уже при обычной температуре по схеме:
HCOOH + ClSO3H → H2SO4 + HCl + CO↑.
2. Нагревание смеси щавелевой и концентрированной серной кислот. Реакция идёт по уравнению:
H2C2O4 →(t, H2SO4) CO↑ + CO2↑ + H2O.
Выделяющийся совместно с CO диоксид углерода можно удалить, пропустив смесь через баритовую воду.
3. Нагревание смеси гексацианоферрата (II) калия с концентрированной серной кислотой. Реакция идёт по уравнению:
K4[Fe(CN)6] + 6H2SO4 + 6H2O →(t) 2K2SO4 + FeSO4 + 3(NH4)2SO4 + 6CO↑.
Применение:
В химической промышленности для синтеза спиртов, углеводородов, альдегидов и органических кислот, а также для получения синтетического жидкого топлива.
Монооксид углерода так же применяется для обработки мяса животных и рыбы, придает им ярко красный цвет и вид свежести, не изменяя вкуса. Допустимая концентрация CO равна 200 мг/кг мяса.
Угарный газ от выхлопа двигателей применялся нацистами в годы Второй мировой войны для массового умерщвления людей путём отравления.
|
Параметры |
Характеристика параметра |
|
Внешний вид |
бесцветный газ |
|
Молекулярная масса (в а.е.м.) |
28 |
|
Температура плавления (в °C) |
−205 |
|
Критическая температура (в °C): |
−140,2 |
|
Температура кипения (в °C) |
−191,5 |
|
Критическое давление (в МПа) |
3,50 |
|
Концентрационные пределы распространения пламени (%) |
12,5 – 74,0 |
|
Плотность (г/см3) |
0,00125 (при 0 °C) |
|
Теплота сгорания (ккал/м3): |
3016 |
|
Стандартная энтальпия образования ΔH (298 К, кДж/моль) |
197,54 |
|
Стандартная мольная теплоемкость Ср (298 К, кДж/моль) |
29,11 |
|
Энтальпия плавления ΔHпл (кДж/моль): |
0,838 |
Основными типами химических реакций, в которых участвует монооксид углерода, являются реакции присоединения и окислительно-восстановительные реакции, в которых он проявляет восстановительные свойства.
При комнатных температурах CO малоактивен, его химическая активность значительно повышается при нагревании и в растворах (так, в растворах он восстанавливает соли Au, Pt, Pd и других до металлов уже при комнатной температуре. При нагревании восстанавливает и другие металлы, например CO + CuO → Cu + CO2↑. Это широко используется в пирометаллургии).
Окисление СО в растворе часто идёт с заметной скоростью лишь в присутствии катализатора. При подборе последнего основную роль играет природа окислителя. Так, KMnO4быстрее всего окисляет СО в присутствии мелкораздробленного серебра, K2Cr2O7 — в присутствии солей ртути, KClO3 — в присутствии OsO4. В общем, по своим восстановительным свойствам СО похож на молекулярный водород. Ниже 830 °C более сильным восстановителем является CO, — выше — водород. Поэтому равновесие реакции:
H2O + CO ↔ CO2 + H2 + 42 кДж
до 830 °C смещено вправо, выше 830 °C влево. Интересно, что существуют бактерии, способные за счёт окисления СО получать необходимую им для жизни энергию.
Монооксид углерода горит синим пламенем (температура начала реакции 700 °C) на воздухе:
