Каталитические мицеллярные эффекты также исчезают в присутствии противоположно заряженных гидрофобных поверхностно-активных веществ. Как видно из рис. 5, кислоты с гидрофобными радикалами средней длины ингибируют гидролиз, скорость которого становится равной скорости гидролиза пропилбетаината. Тетрадекановая кислота почти полностью останавливает гидролиз при концентрации ниже 5 мМ. Этот эффект объясняется образованием смешанных мицелл тетрадецилбетаината и тетрадеканоата. Выше некоторой концентрации тетрадеканоата заряд мицелл становится отрицательным, что приводит к отталкиванию между гидроксид-ионами и мицеллярной поверхностью.
Микроэмульсии как растворители для органического синтеза
Использование микроэмульсий в органическом синтезе оказалось чрезвычайно полезным, поскольку они способны солюбилизировать полярные и неполярные компоненты, а также пространственно разделять или концентрировать реагенты. Дальнейшее обсуждение использования микроэмульсий можно разделить на три направления: а) решение проблемы несовместимости реагентов, б) реакции, где достигается специфический каталитический эффект, в) регулирование ре-гиоселективности реакций.
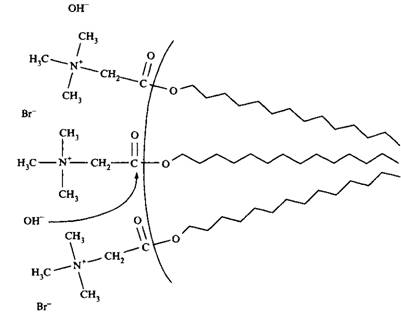
Рис. 4. Мицеллярный катализ обусловлен высокими концентрациями реагентов на поверхности мицеллы. Гидроксид-ионы могут вытесняться не участвующими в реакции ионами, например бромид-ионами, тогда каталитический эффект исчезает
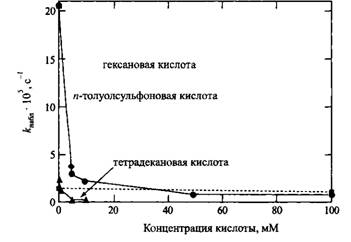
Рис. 5. Влияние гидрофобных поверхностно-активных кислот на константу скорости гидролиза тетрадецилбетаината; пунктирная линия — гидролиз пропилбетаината
Решение проблемы несовместимости реагентов
В органическом синтезе одной из распространенных практических проблем является достижение эффективного контакта между неполярными органическими компонентами и неорганическими солями. Существует множество примеров важных реакций, в которых исследователи сталкиваются с этой проблемой: щелочной гидролиз сложных эфиров, окислительное расщепление олефинов перманганатом и периодатом, присоединение групп HSCb- к альдегидам и концевым алкеновым связям, получение алкилсульфонатов при взаимодействии алкилхлоридов с сульфитами или при присоединении гидросульфит-иона к б-олефиноксидам. Этот список можно продолжить. Для всех приведенных примеров характерна общая проблема совместимости реагентов, особенно если органический компонент представлен большими неполярными молекулами.
Сейчас уже разработаны различные пути решения проблемы плохого межфазного контакта, затрудняющего проведение реакций органического синтеза. Один из них — использование растворителя или смеси растворителей, способных растворять как органическое соединение, так и неорганические соли. Для этой цели иногда пригодны полярные апротонные растворители, но большинство из них не подходят для крупномасштабных производств либо из-за токсичности, либо из-за трудности их удаления вакуумной перегонкой.
Альтернативный путь заключается в проведении реакций в системах с двумя несмешивающимися растворителями. При этом площадь межфазного контакта можно увеличивать путем перемешивания. При проведении реакций в двухфазных системах полезно использовать реагенты, обладающие свойствами межфазных переносчиков. Такими свойствами обладают четвертичные аммониевые соединения и краун-эфиры. Последние оказались также весьма эффективны для решения проблемы контакта разнородных фаз, однако их использование ограничено высокой стоимостью. Полиоксиэтиленовые соединения с открытыми цепями часто обнаруживают эффекты, аналогичные описанным для краун-эфи-ров, и могут представлять практический интерес как альтернативные реагенты, обеспечивающие межфазный перенос.
Микроэмульсии одинаково хорошо растворяют гидрофобные органические вещества и неорганические соли. Эти макроскопически гомогенные системы в микроскопическом масштабе представляют собой дисперсии и могут рассматриваться как промежуточные системы между однофазными растворами и истинно двухфазными системами. В связи с этим микроэмульсии являются альтернативой двухфазных систем с межфазными переносчиками. Сказанное можно показать на примере микроэмульсий, использующихся для детоксикации горчичного газа.
Горчичный газ — широко известный представитель химического оружия. Несмотря на то, что в лабораторных условиях он подвержен быстрой гидролитической дезактивации, когда скорости измеряются при низких концентрациях субстрата, на практике его дезактивация происходит не столь легко. Из-за очень низкой растворимости в воде горчичный газ в течение многих месяцев остается на поверхности воды. Добавление каустической соды не приводит к заметному увеличению скорости его гидролитического распада. Микроэмульсии были исследованы в качестве сред для гидролиза и окисления «полугорчичного» газа — вещества, моделирующего горчичный газ. Оказалось, что окисление гипохлоритом протекает чрезвычайно быстро как в микроэмульсиях «масло в воде», так и «вода в масле». В микроэмульсиях, основанных на ПАВ любого типа, полное окисление «полугорчичного газа» до сульфоксида происходило не более чем за 15 с. Эта реакция протекает за 20 мин в двухфазных системах в присутствии межфазных переносчиков.
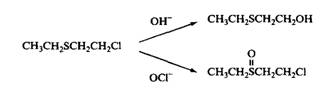
Рис. 6. Превращение 2-хлорэтилсульфида: в 2-гидроксиэтил-сульфид в щелочной среде и в 2-хлорэтилсульфоксид под действием гипохлорита натрия
Микроэмульсии как реакционные среды можно использовать в качестве альтернативы катализа с фазовым переносом. При этом наилучших результатов добиваются при комбинации обоих подходов. Скорость реакции
![]()
резко повышается, если ее проводить в микроэмульсии с добавлением катализатора фазового переноса
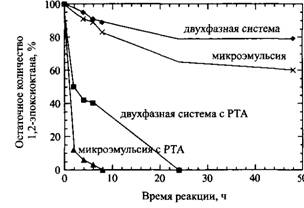
Рис. 7. Скорость реакции раскрытия цикла липофильного эпоксида под действием гидросульфита. Реакция проведена в двухфазной системе и в микроэмульсиях без добавок и в присутствии межфазного переносчика
Для проведения реакций органического синтеза совсем не обязательно использовать однофазные микроэмульсии. Установлено, что для большинства реакций подходят системы Винзора I или Винзора III. В таких системах скорость переноса реагентов между микроэмульсионной фазой, в которой протекает реакция, и избытком масла или воды намного превышает скорость реакции. Это важно с практической точки зрения, поскольку облегчает составление микроэмульсионных композиций. Составление композиций для получения микроэмульсий типа Винзора I или Винзора III намного проще, чем для получения однофазной микроэмульсии с участием всех компонентов реакционной смеси.
Специфическое увеличение скорости реакции
Соответствующим подбором ПАВ можно добиться такого же увеличения скорости, как при мицеллярном катализе. Этот эффект называют микроэмульсионным катализом.
