Стандартные режимы работы. В стандартных ОСК два главных рабочих режима: покраски и сушки. В первом случае воздух берется с улицы, нагревается, подается в кабину и тут же выбрасывается обратно в атмосферу. Его температура: + 20… + 25 0С. Все стандартные ОСК вне зависимости от производителя работают с внешним воздухом, температура которого не может опускаться ниже определенного значения. Разница температур на улице и внутри ОСК, как правило, колеблется от + 27 до + 35 0С. При температуре «за бортом» ниже требуемой мы не достигнем в кабине оптимальной для рабочего режима температуры. Есть два метода, чтобы как-то поправить положение: во-первых, устанавливают смешивающее заборное устройство (с улицы и непосредственно из помещения станции), во-вторых, ставится система рекуперации (нагрев входящего воздуха выходящим).
Второй режим работы ОСК — режим сушки. Температура поддерживается на уровне + 60 0С. В этом режиме камера работает в режиме рециркуляции, т. е. воздух обращается по замкнутому циклу: генераторная группа — кабина — экстракторная группа — генераторная группа — и т.д. В этом случае до 90 % используемого воздуха прогоняется в ОСК повторно и только около 10 % забирается с улицы.
Между режимом покраски и режимом сушки существует еще переходный режим — испарения растворителя. Ведь если мы резко поднимем температуру после окраски, то верхний слой лакокрасочного материала просто запечется, а нижний останется сырым, что послужит причиной брака. Чтобы этого не происходило, набор температуры производится после испарения растворителя.
Физико-химические свойства обращающихся в помещениях цеха веществ и материалов
Характеристика бензола
БЕНЗОЛ (С6Н6), молярная масса равна 78,11; бесцветная жидкость с характерным запахом; температура плавления 5,53°С, температура кипения 80,1°С; энтальпия плавления 9,843 кДж/моль, энтальпия испарения 30,77 кДж/моль, энтальпия сгорания - 3303,72 кДж/моль, энтальпия образования - 82,98 кДж/моль; давление критическое 4,91 МПа, температура критическая 289,5 °С. Растворимость в воде 0,073% по массе (25 °С), воды в бензоле 0,05% (26 °С). Неограниченно растворяется в углеводородах, эфирах, хуже – в метаноле, не растворяется в этиленгликоле, глицерине; растворяет жиры, каучуки, гудрон, серу, фосфор,иод.
Молекула бензола - плоский правильный шестиугольник с внутренними углами 120° и расстоянием между атомами углерода 0,139 нм.
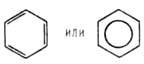
Бензол - родоначальник углеводородов ароматического ряда. Химические свойства определяются наличием в молекуле стабильной замкнутой системы ![]() электронов. Он склонен к донорно-акцепторному взаимодействию с соединениями, имеющими дефицит электронов; в результате образуются малостабильные и существующие только в растворах
электронов. Он склонен к донорно-акцепторному взаимодействию с соединениями, имеющими дефицит электронов; в результате образуются малостабильные и существующие только в растворах ![]() комплексы, которые могут превращаться в более прочные
комплексы, которые могут превращаться в более прочные ![]() комплексы.
комплексы.
Для бензола характерна устойчивость к действию высоких температур и окислителей. Лишь выше 650°С он частично превращается в дифенил, выше 750°С разлагается на углерод и водород. Бензол не изменяется под действием Н2СrO4 и КМnО4, с О2 в присутствии катализаторов (V, Мо) при 350-450°С образует малеиновый ангидрид. Гидрируется до циклогексана в присутствии различных катализаторов (например, в присутствии Ni при 120-200°С и 2,96-6,94 МПа). Щелочными металлами в жидком NH3 восстанавливается до 1,4-циклогексадиена. При фотохимическом присоединении хлора превращается в гексахлорциклогексан. При УФ-облучении способен к циклоприсоединению и изомеризации в фульвен и бензвален.
Наиболее старый метод промышленного получения бензола: выделение его из предварительно охлажденных пирогазовых продуктов коксования каменных углей абсорбцией органическими поглотителями, например, маслами каменно-угольного и нефтяного происхождения; для отделения поглотителя используют перегонку с водяным паром. От примесей (напр., тиофена) сырой бензол отделяют гидроочисткой. Основное количество бензола получают риформингом (470-550°С) нефтяной фракции, выкипающей при 62-85 °С; извлекают экстракцией. Бензол высокой чистоты получают экстрактивной перегонкой с ДМФА. Бензол выделяют также из жидких продуктов пиролиза нефтепродуктов, образующихся в производстве этилена и пропилена. При избытке ресурсов толуола бензол производят деалкилированием последнего, которое проводят термическим способом при 600-820°С в присутствии Н2 и водяного пара или каталитически при 227-627°С в присутствии цеолитов или оксидных катализаторов. В лабораториях особо чистый бензол синтезируют декарбоксилированием бензойной кислоты.
Основные области применения бензола (более 80%): производство этилбензола, кумола и циклогексана; остальное количество - для получения анилина, малеинового ангидрида, как компонент моторного топлива для повышения октанового числа, как раствоитель и экстрагент в производстве лаков, красок, ПАВ и др.
Транспортируют в железнодорожных цистернах, снабженных оборудованием для разогрева продукта. Бензол открыт М. Фарадеем в 1825 г. при пиролизе китового жира; впервые синтезирован Э. Мичерлихом в 1833 г. декарбоксилированием бензойной кислоты.
Для бензола температура вспышки - 11 °С, температура самовоспламенения 534°С, КПВ 1,5-8%. Сильно раздражает кожу; в высоких концентрациях бензол оказывает судорожное действие; при многократных воздействиях низких концентраций наблюдаются изменения в крови и кроветворных органах; ПДК 5 мг/м3. Смертельная концентрация в крови 0,9 мг/л. Быстро всасывается в легких, желудочно-кишечном тракте.
Симптомы:
При вдыхании паров бензола - возбуждение, подобное алкогольному, судороги, бледность лица, слизистые оболочки красного цвета, зрачки расширены. Одышка. Снижение артериального давления, возможно кровотечение из носа, десен, маточные кровотечения, явления паралича дыхательного центра. Смерть может наступить от остановки дыхания и падения сердечной деятельности. При приеме бензола внутрь возникают боли в животе, рвота, явления поражения печени (желтуха и тд.).
Лечение:
Удалить пострадавшего из опасной зоны. Промывание желудка через зонд, вазелиновое масло внутрь - 200 мл, солевое слабительное - 30 г сульфата натрия (глауберова соль). Форсированный диурез. Операция замещения крови. 30 % раствор тиосульфата натрия - 200 мл внутривенно. Ингаляция кислорода. Симптоматическая терапия.
Расчет избыточного давления взрыва для индивидуальных горючих газов, паров легковоспламеняющихся и горючих жидкостей
Алгоритм расчета
Избыточное давление взрыва ∆Р для индивидуальных горючих веществ, состоящих из атомов С, Н, О, Cl, Br, I, F определяется по формуле (1):
![]() (1)
(1)
